"REPLICACIÓN DEL ADN”
ALUMNO:CANDIDO TORRES SANTIBAÑEZ.
CON # DE CONTROL:09930058.
PROFESOR: JAVIER FRANCISCO PUCHE ACOSTA.
14/03/2012.
UNIDAD # 4
“REPLICACIÓN DEL ADN”
4.1 REPLICACIÓN DEL
GENOMA PROCARIÓTICO
4.2 REPLICACIÓN DEL
GENOMA EUCARIÓTICO
4.3 CONTROL GENÉTICO
DE LA REPLICACIÓN.
4.4 REPLICACIÓN IN
VITRO DEL ADN (PCR)
4.4.1 SECUENCIACIÓN
DEL ADN
INTRODUCCION
El proceso de replicación de ADN es el mecanismo que permite al ADN duplicarse (es decir, sintetizar una copia idéntica).
De esta manera de una molécula de ADN única, se obtienen dos o más "clones" de la primera.
Esta duplicación del material genético se produce de acuerdo con un mecanismo semiconservativo, lo que indica que las dos cadenas complementarias del ADN original, al separarse, sirven de molde cada una para la síntesis de una nueva cadena complementaria de la cadena molde, de forma que cada nueva doble hélice contiene una de las cadenas del ADN original.
Gracias a la complementacion entre las bases que forman la secuencia de cada una de las cadenas, el ADN tiene la importante propiedad de reproducirse idénticamente, lo que permite que la información genética se transmita de una célula madre a las células hijas y es la base de la herencia del material genético.
La molécula de ADN se abre como una cremallera por ruptura de los puentes de hidrógeno entre las bases complementarias liberándose dos hebras y la ADN polimerasa sintetiza la mitad complementaria añadiendo nucleótidos que se encuentran dispersos en el núcleo. De esta forma, cada nueva molécula es idéntica a la molécula de ADN inicial.
La replicación empieza en puntos determinados: los orígenes de replicación.
Las proteínas iniciadoras reconocen secuencias de nucleótidos específicas en esos puntos y facilitan la fijación de otras proteínas que permitirán la separación de las dos hebras de ADN formándose una horquilla de replicación.
Un gran número de enzimas y proteínas intervienen en el mecanismo molecular de la replicación, formando el llamado complejo de replicación o replisoma.
Estas proteínas y enzimas son homólogas en eucariotas y arqueas, pero difieren en bacterias.
En cada una de las moléculas hijas se conserva una de las cadenas originales, y por eso se dice que la replicación del ADN es semiconservadora. Hasta que finalmente se pudo demostrar que la replicación es semiconservadora, se consideraron tres posibles modelos para el mecanismo de la replicación:
- Semiconservadora (modelo correcto). En cada una de las moléculas hijas se conserva una de las cadenas originales.
- Conservadora. Se sintetiza una molécula totalmente nueva, copia de la original.
- Dispersora, o dispersante. Las cadenas hijas constan de fragmentos de la cadena antigua y fragmentos de la nueva.
Para ello se hicieron crecer células de Escherichia coli en presencia de nitrógeno-15, un isótopo del nitrógeno más pesado de lo habitual.
En consecuencia, el isótopo se incorporó a las cadenas de ADN que se iban sintetizando, haciéndolas más pesadas.
Una vez conseguido el primer objetivo, las células fueron transferidas a un medio que contenía nitrógeno-14, es decir, un medio más ligero, donde continuaron su crecimiento (división celular, que requiere la replicación del ADN).
Se purificó el ADN y se analizó mediante una centrifugación en gradiente de cloruro de cesio, en donde hay más densidad en el fondo del tubo que en la parte media del mismo.
En la primera generación (figura 2.b) se obtuvo una única banda de ADN con densidad intermedia. En la segunda generación (figura 2.c) se obtuvieron dos bandas, una con densidad ligera y otra con densidad intermedia o híbrida.
En la tercera generación se obtuvieron dos bandas, una ligera (con una abundancia del 75%) y otra intermedia (con el 25% restante).
La banda intermedia o híbrida representa una molécula de ADN que contiene una cadena pesada (original) y otra ligera (recién sintetizada).
Las cadenas ligeras representan una molécula de ADN en la que las dos cadenas han sido sintetizadas (no existían aun cuando las células se pusieron en presencia de nitrógeno-15.
El hecho de que cada vez haya más moléculas ligeras y se mantenga el número de moléculas intermedias demuestra que la del ADreplicación N es semiconservadora.
Si fuera conservadora, aparecería siempre una banda pesada y el resto ligeras (figuras 1.a, 1.b, 1.c) . Si fuera dispersante sólo aparecerían bandas híbridas de densidad intermedia en todas las generaciones
APORTACIÓN DE LA
ASIGNATURA AL PERFIL DEL EGRESADO
Comprender las bases
moleculares que rigen el control de los procesos celulares como la expresión
génica, la muta génesis y reparación del ADN así como los mecanismos de
transferencia, recombinación y técnicas para conocer su aplicación en la
manipulación del material genético con fines biotecnológicos.
OBJETIVO(S)
GENERAL(ES) DEL CURSO
Entenderá las bases moleculares del control de la expresión génica y de la manipulación del ADN mediante el empleo de las diferentes técnicas moleculares que le permitan desarrollar proyectos de investigación básica y aplicada.
OBJETIVOS EDUCASIONALES O ESPECIFICOS.
Entenderá como se
transmite la información genética entre
los seres vivos y su relación con los mecanismos de herencia.
Distinguirá los
mecanismos de duplicación del material
genético en procariotas y
Eucariotas.
METODOLOGIA
( DESENLACE DE LA UNIDAD TEMAS VISTOS EN CLASES INPARTIDOS Y EXPLICADOS POR EL PROFESOR POR EL PROFESOR.
UNIDAD 4 REPLICACIÓN
DEL ADN
El modelo que explica cómo se duplica el DNA se denomina modelo semiconservativo ya que a partir de una molécula de ADN obtendremos dos exactamente iguales, cada una con una hebra antigua (cadena parda en la imagen siguiente) y otra nueva (cadena naranja en la imagen siguiente): la cadena original comienza a separarse de un extremo a otro de modo que cada una de las hélices va a sintetizar una hélice nueva complementaria habiendo tomado como modelo o patrón a la hélice inicial.
Al incorporarse el NTP, se liberan dos de los tres fosfatos para aportar la energía necesaria a la reacción química.
Las DNA-polimerasas sólo funcionan utilizando un DNA como molde, necesitando inexcusablemente un cebador (pequeño oligonucleótido de
Los nucleótidos se van añadiendo en el extremo
La DNA-polimerasa no comienza a replicar ni al azar ni en cualquier parte.
Un complejo sistema de regulación intracelular le indica el momento del ciclo celular en que debe comenzarse la replicación, la enzima reconoce una secuencia de nucleótidos llamada origen de replicación que marca el punto el que ha de comenzarse la replicación.
En Escherichia coli es la secuencia de 245 pares de bases que tiene varias repeticiones de una secuencia consenso GATCTNTTNTTT.
Meselson y Stahl confirman en 1958 que la síntesis del DNA es
semiconservativa partiendo de un DNA con gran contenido de [15N].
En el caso de E. coli, se observa que el origen de replicación es rico en A y T para que cueste menos energía separar las cadenas.
La separación de las dos cadenas provoca una serie de tensiones topológicas en el DNA que hacen necesaria la intervención de otras enzimas, las topoisomerasas, para eliminar dichas tensiones.Se forma así una burbuja de replicación con un ADN desapareado flanquedado por sendos ADN apareados.
Como el proceso es bidireccional, a cada extremo de la burbuja se forma una horquilla de replicación de manera que las dos hebras se van copiando a la par.

Antes de que la
DNA-polimerasa añada el primer nucleótido interviene una DNA-polimerasa
denominada primasa que sintetiza un corto fragmento de RNA de
10 nucleótidos que actúa de cebador.
El cebador es elongado por la DNA-polimerasa en dirección 5´->3´. Una de las dos hebras, la hebra conductora es de crecimiento continuo puesto que la horquilla se va abriendo en el mismo sentido que la DNA-polimerasa añade los nucleótidos.
La otra cadena (hebra retrasada) transcurre en sentido opuesto, por lo que ha de seguir un proceso un poco diferente para replicarse.
En ella la primasa sintetiza el cebador a 1000 nucleótidos del punto de separación del DNA progenitor.
A partir del cebador la DNA-polimerasa sintetiza unos 1000 nucleótidos de DNA, alejándose de la horquilla de replicación, formándose el denominado fragmento de Okazaki. Después, otra DNA-polimerasa distinta retira los fragmentos de RNA que han hecho de cebador y rellena los huecos con nucleótidos de DNA.
Finalmente la ADN-ligasa empalma entre sí los diferentes fragmentos para formar una cadena única a partir de los fragmentos de Okazaki; por eso se dice que es una replicación discontinua. El proceso continúa hasta que se duplica todo el DNA.
El conjunto de proteínas que se forman el punto de bifurcación de la horquilla se conoce como replisoma. Es mejor conocido es el replisoma de E. coli.
El cebador es elongado por la DNA-polimerasa en dirección 5´->3´. Una de las dos hebras, la hebra conductora es de crecimiento continuo puesto que la horquilla se va abriendo en el mismo sentido que la DNA-polimerasa añade los nucleótidos.
La otra cadena (hebra retrasada) transcurre en sentido opuesto, por lo que ha de seguir un proceso un poco diferente para replicarse.
En ella la primasa sintetiza el cebador a 1000 nucleótidos del punto de separación del DNA progenitor.
A partir del cebador la DNA-polimerasa sintetiza unos 1000 nucleótidos de DNA, alejándose de la horquilla de replicación, formándose el denominado fragmento de Okazaki. Después, otra DNA-polimerasa distinta retira los fragmentos de RNA que han hecho de cebador y rellena los huecos con nucleótidos de DNA.
Finalmente la ADN-ligasa empalma entre sí los diferentes fragmentos para formar una cadena única a partir de los fragmentos de Okazaki; por eso se dice que es una replicación discontinua. El proceso continúa hasta que se duplica todo el DNA.
El conjunto de proteínas que se forman el punto de bifurcación de la horquilla se conoce como replisoma. Es mejor conocido es el replisoma de E. coli.
PROCESO GENERAL.
- La helicasa rompe los puentes de hidrógeno de la doble hélice permitiendo el avance de la horquilla de replicación.
- La topoisomerasa impide que el ADN se enrede debido al superenrollamiento producido por la separación de la doble hélice.
- Las proteínas SSB se unen la hebra discontínua de ADN, impidiendo que ésta se una consigo misma.
- La ADN polimerasa sintetiza la cadena complementaria de forma continua en la hebra adelantada y de forma discontínua en la hebra rezagada.
- La ARN primasa sintetiza el cebador de ARN necesario para la síntesis de la cadena complementaria a la cadena rezagada.
- La ADN ligasa une los fragmentos de Okazaki.
- El cebador: son pequeñas unidades de RNA que se unen a los fragmentos para que la ADN polimerasa reconozca donde debe unirse.
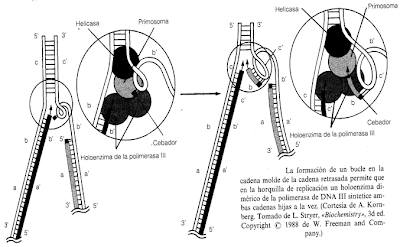
La biosíntesis de la
hebra guía y rezagada esta coordinada, por que la hebra rezagada forma un bucle
de manera que físicamente apunta en la
misma dirección que la hebra guía. Esto significa que ambas hebras tiene un
acceso similar a la enzima polimerasa.
Estructuras en q
La replicación del DNA circular produce las llamadas estructura en q que se forma como resultado de las dos horquillas de replicación.
La replicación se da simultáneamente en la dirección de las manecillas del reloj y en la dirección contraria. Para exponer las hebras sencillas de DNA, las dos hebras progenitoras deben girar. Por cada 10 bases que se copian el DNA debe dar 1 vuelta completa.
Puede calcularse que en E. coli la horquilla de replicación necesita moverse a a una velocidad de 800 bases por segundo, lo que requiere que el DNA progenitor se desenrolle a razón de 80 revoluciones por segundo.
La replicación semiconservativa del DNA requiere que se produzca un corte en uno o en ambos nucleótidos del esqueleto para aliviar la tensión en la molécula, esta labor la hace las topoisomerasas.
La topoisomerasa I cambia el DNA superenrrollado a un DNA relajado, La topoisomerasa II (girasas) produce hélices negativas al destorcer el DNA
4.1 REPLICACION DEL GENOMA PROCARIOTICO.
1ª etapa: desenrrollamiento y apertura de la doble hélice.en el punto ori-c.
Intervienen un grupo de enzimas y proteinas, a cuyo conjunto se denomina replisoma
* Primero: intervienen las helicasas que facilitan en desenrrollamiento
* Segundo: actuan las girasas y topoisomerasas que eliminan la tensión generada por la torsión en el desenrrollamiento.
* Tercero: Actuan las proteinas SSBP que se unen a las hebras molde para que no vuelva a enrollarse.
* Actuan las ADN polimerasas para sintetizar las nuevas hebras en sentido 5´-3´, ya que la lectura se hace en el sentido 3´-5´.
* Intervienen las ADN polimerass I y III, que se encargan de la replicación y corrección de errores. La que lleva la mayor parte del trabajo es la ADN polimerasa III
* Actua la ADN polimerasa II, corrigiendo daños causados por agentes físicos.
La cadena 3´-5´es leida por la ADN polimerasa III sin ningún tipo de problemas ( cadena conductora). En la cadena 5´-3´ no puede ser leida directamente, esto se soluciona leyendo pequeños fragmentos ( fragmentos de Okazaki ) que crecen en el sentido 5´-3´y que más tarde se unen . Esta es la hebra retardada,llamada de esta forma porque su síntesis es más lenta.
La ADN polimerasa III es incapaz de iniciar la síntesis por sí sola, para esto necesita un cebador (ARN) que es sintetizado por una ARN polimerasa (=primasa). Este cebador es eliminado posteriormente.
3ª etapa: corrección de errrores.
El enzima principal que actua como comadrona (R. Shapiro) es la ADN polimerasa III, que corrige todos los errores cometidos en la replicación o duplicación. Intervienen otros enzimas como:
* Endonucleasas que cortan el segmento erroneo.
* ADN polimerasas I que rellenan correctamente el hueco.
* ADN ligasas que unen los extremos corregidos
Aunque las
actividades enzimáticas sean las mismas en procariotas y eucariotas, hay muchas
más proteínas implicadas en la replicación de los eucariotas.
Por otro lado, el DNA eucariótico tiene más problemas con el superenrollamiento al estar muy estrechamente asociado a unas proteínas denominadas histonas.
También es distinto el hecho de que en un cromosoma procariótico sólo hay un origen de replicación en el único cromosoma, mientras que en los de eucariotas suele haber muchos más (a veces más de 30.000) por cada cromosoma.
Los múliples orígenes de replicación en eucariotas asegura que el genoma se puede replicar en muy poco tiempo.
Por otro lado, el DNA eucariótico tiene más problemas con el superenrollamiento al estar muy estrechamente asociado a unas proteínas denominadas histonas.
También es distinto el hecho de que en un cromosoma procariótico sólo hay un origen de replicación en el único cromosoma, mientras que en los de eucariotas suele haber muchos más (a veces más de 30.000) por cada cromosoma.
Los múliples orígenes de replicación en eucariotas asegura que el genoma se puede replicar en muy poco tiempo.
DNA polimerasas procariotas
Las DNA polimerasas I, II y III se encuentran en las procariontes.
En la siguiente tabla se resumen las propiedades de las diferentes enzimas.
Propiedades de la DNA polimerasa de E: coli y de
retrovirus
Polimerasa
|
E. coli
|
Virus*
|
||||
I
|
II
|
III
|
||||
Mr
|
109 000
|
120 000
|
180 000
|
160 000
|
||
Estructura, subunidades, Mr
|
una
|
una
|
a 140 000
|
a 65 000
|
||
e 25 000
|
b 95 000
|
|||||
q 10 000
|
||||||
+
|
+
|
+
|
+
|
|||
Actividad exonucleasa
|
||||||
+
|
-
|
+
|
-
|
|||
+
|
+
|
+
|
-
|
|||
virus de la mieloblastosis avícola, un retrovirus
La DNA polimerasa I de E.
coli es una sola cadena polipeptídica de Mr 109 000. Contiene un átomo de zinc
por molécula. Cataliza la polimerización en el sentido 5´ 3´.
LA DNA polimerasa III de E. coli esta formada por 7
subunidades: a,
b,
g,
d,
e,
q
y t.
Las siete son escenciales para la actividad máxima.
La DNA pol. III es la principal enzima de replicación en
E. coli. La DNA pol. I es responsable de la reparación de DNA dañado. La
funcion de la DNA pol II no esta todavía clara.
DNA polimerasas eucariotas
Polimerasa
|
a
|
b
|
g
|
d
|
e
|
Mr
|
300 000
|
45 000
|
140 000
|
180-240 000
|
290 000
|
Composición de la
subunidad
|
4
|
1
|
4
|
2
|
2
|
Sitio
Actividad polimerasa
|
Núcleo
Replicación del DNA
cromosomal
(hebra rezagada)
|
Núcleo
Reparación
|
Mitocondrias
Replicación del DNA
mitocondrial
|
Núcleo
Replicación del DNA cromosomal
(hebra guía)
|
Núcleo
Replicación del DNA
cromosomal
Reparación del DNA dañado
por la radiación UV.
|
Actividad exonucleasa
|
-
|
-
|
-
|
+
|
+
|
Se conocen cinco polimerasas eucariontes (a, b, g, d y e.) y tienen un mecanismo de acción similar al de las enzimas procariotes.
Las DNA pol. a y d son las que están asociadas mas directamente ala replicación del DNA cromosómico.
La DNA pol. b es responsable de la reparación del DNA. L DNA pol. g se encuentra en las mitocondrias y se encarga de replicar el DNA mitocondrial. La DNA pol. e es recién descubierta y se asemeja en funciones a d.
Los retrovirus contienen RNA y no DNA como material genético, y tienen una DNA polimerasa dependiente del RNA (una trascriptasa inversa).
hay 1 lugar de origen de replicación que se muestra en la horquilla de replicación (replication fork) y que señala el avance de la copia.
4.2. REPLICACION DEL ADN EN EUCARIONTES.
Es similar a la de los procariontes, es decir, semiconservativa y bidireccional. Existe una hebra conductora y una hebra retardada con fragmentos de Okazaki. Se inicia en la burbujas de replicación (puede haber unas 100 a la vez)
Intervienen enzimas similares a los que actuan en las células procariontes y otros enzimas que han de duplicar las histonas que forman parte de los nucleosomas. Los nucleosomas viejos permanecen en la hebra conductora.
El mecanismo para la
síntesis del DNA en eucariontes probablemente es similar al proceso en
procariontes.
Las principales complicaciones adicionales son que el DNA en eucariontes se organiza en varios cromosomas lineales y que el DNA es mucho más largo que el que se encuentra en los procariontes.
El movimiento de la DNA polimerasa es mucho más lento que en los procariontes; para compensar esto, una célula eucarionte tiene mas o menos 20 000 moléculas de la enzima. Esto permite que se forme un numero mayor de horquillas de replicación, por ejemplo 2000 o más, en los cromosomas eucariontes. También se forman fragmentos de okazaki más pequeños, con longitud de 40 a 300 bases.
De esta manera en
general la replicación del DNA es mucho más rápida que la de E. coli.
Terminación de la
replicación: síntesis de los telómeros
El final de la
replicación en eucariotas tiene que resolver el problema del acortamiento de
los cromosomas. Para ello ha desarrollado la estructura de los telómeros y
telosomas, y la actuación de una nueva enzima emparentada con las
retrotranscriptasas: la telomerasa.
En las células eucariotas el proceso es esencialmente el mismo pero el ADN es mucho más grADNe y linear. Hay varios orígens de replicación y es bidireccional. El avance es más lento que en procariotas ya que hay más proteínas asociadas al ADN que hay que soltar. La replicación del ADN, que ocurre una sola vez en cada genración celular necesita de muchos "ladrillos", enzimas y una gran cantidad de energía en forma de ATP (recuerde que luego de la fase S del ciclo celular , las células pasan a una fase G a fin de, entre otras cosas, recuperar energía para la siguiente fase de la división celular). La replicación del ADN en el ser humano se realiza a una velocidad de 50 nucleótidos por segundo. Los nucleótidos tienen que ser armados y estar disponibles en el núcleo conjuntamente con la energía para unirlos. Una vez que se abre la molécula, se forma una área conocida como "burbuja de replicación" en ella se encuentran las "horquillas de replicación" . Por acción de la la ADN polimerasa los nuevos nucleótidos entran en la horquilla y se enlazan con el nucleótido correspondiente de la cadena de origen (A con T, C con G). Los procariotas abren una sola burbuja de replicación, mientras que los eucariotas múltiples. El ADN se replica en toda su longitud por confluencia de las "burbujas". Dado que las cadenas del ADN son antiparalelas, y que la replicación procede solo en la dirección 5' to 3' en ambas cadenas, numerosos experimentos han mostrado que, una cadena formará una copia continua, mientras que en la otra se formarán una serie de fragmentos cortos conocidos como fragmentos de Okazaki . La cadena que se sintetiza de manera continua se conoce como cadena guía, delantera ó adelantada y, la que se sintetiza en fragmentos, cadena atrasada ó rezagada. Los fragmentos cortos, recién sintetizados de hebras de ADN se denominan fragmentos Okazaki. Todas las ADN polimerasas conocidas, pueden sólo sintetizar ADN en la dirección 5' a 3' . Sin embargo, cuADNo las hebras se separan, la horquilla de replicación se desplaza a lo largo de una hebra molde en la posición 3' a 5' y 5' a 3' en el otro lado del molde. En la primera , la cadena adelantada de ADN es sintetizada continuamente en la dirección 5' a 3'. En la otra, llamada la cadena atrasada, la síntesis de ADN sólo ocurre cuando ADNo una sección de una hebra simple de ADN ha sido expuesta y procede en la dirección opuesta a la dirección de la horquilla de replicación (5' to 3'). Es por ésto discontinua y la serie de fragmentos Okazaki son unidos de manera covalente por las ligasas formADNo una hebra continua. Se denominan fragmentos Okazaki porque fué éste investigador quien primeramente los observó y estudió usADNo timidina radioactiva . En los eucariotas, los fragmentos Okazaki están formados por unos cuantos cientos de nucleótidos, mientras que en los procariotas estos fragmentos pueden alcanzar algunos miles Para que la ADN polimerasa trabaje, se necesaria la presencia, en el inicio de cada nuevo fragmento, de pequeñas unidades de ARN conocidas como cebadores, a posteriori, cuADNo la polimerasa toca el extremo 5' de un cebador, se activan otras enzimas, que remueven los fragmentos de ARN, colocan nucleótidos de ADN en su lugar y una ADN ligasa que los une a la cadena en crecimiento. |
4.3. CONTROL GENETICO DE LA REPLICACION.
El código genético viene a ser como un diccionario
que establece una equivalencia entre las bases nitrogenadas del ARN y el leguaje
de las proteinas, establecido por los aminoácidos.
Después de muchos estudios (1955 Severo Ochoa y
Grumberg; 1961 M.Nirenberg y H. Mattaei) se comprobó que a cada aminoácido la
corresponden tres bases nitrogenadas o tripletes (61 tripletes codifican
aminoácidos y tres tripletes carecen de sentido e indican terminación de
mensaje).
El código genético tiene una serie de
características:
- Es universal, pues lo utilizan casi todos los seres vivos conocidos. Solo
existen algunas excepciones en unos pocos tripletes en
bacterias.
-o es ambigüo, pues cada triplete tiene su propio significado
- Todos los tripletes tienen sentido, bien codifican un aminoácido o bien
indican terminación de lectura.
- Está degenerado, pues hay varios tripletes para un mismo aminoácido, es
decir hay codones sinónimos.
- Carece de solapamiento,es decir los tripletes no comparten bases
nitrogenadas.
- Es unidireccional, pues los tripletes se leen en
el sentido 5´-3´.
La mayor parte de los estudios de ciclo celular se han llevado a cabo empleando S. cerevisiae, la levadura del pan y la cerveza también conocida como la levadura de gemación por su característico estilo de división. En el caso de este organismo hay que añadir la ventaja de que actualmente se conocen los aproximadamente 16 millones de pares de nucleótidos que constituyen la secuencia completa de su genoma.
| Figura : Ciclo
celular de S. cerevisiae |
Los fundamentos de nuestro conocimiento actual del ciclo celular en levaduras vienen de la búsqueda sistemática de mutaciones en genes que codifican para componentes de la maquinaria del ciclo.
Estos estudios han
permitido identificar una familia de proteínas quinasas dependientes de
ciclina, -Cyclin Dependent Kinases, Cdk- que incluyen a Cdc28 de S. cerevisiae,
y a su homólogo en S. pombe cdc2, y que juegan un papel central en los
procesos claves del ciclo celular: la entrada en ciclo, la síntesis de ADN y la
regulación de la mitosis.
Estas quinasas son las subunidades catalíticas de un complejo que incluye también na subunidad reguladora, denominada ciclina, necesaria para la función del complejo al determinar la localización o la especificidad de sustrato de la quinasa.
Estas quinasas son las subunidades catalíticas de un complejo que incluye también na subunidad reguladora, denominada ciclina, necesaria para la función del complejo al determinar la localización o la especificidad de sustrato de la quinasa.
En los últimos años se han encontrado también homólogos a estas quinasas en todos los eucariotas en los que se han buscado, y que incluyen desde el gusano nematodo Caenorhabditis elegans, a la mosca Drosophila melanogaster , a mamíferos como el ratón y el hombre y plantas como Arabidopsis thaliana, indicando que el sistema de control del ciclo celular es general en todos los eucariotas y validando a las levaduras como modelos de estudio.
4.4 REPLICACION IN VITRO DEL ADN (PCR).
La
Reacción en Cadena de la Polimerasa (PCR) es una técnica de laboratorio que
permite la copia in vitro de secuencias específicas de DNA y que ha
revolucionado el campo de la Biología Molecular.
Conceptualmente, la PCR es una técnica sencilla, consiste en la separación por calor de las dos cadenas del DNA que se quiere amplificar, y su copia simultánea a partir de un punto, determinado por un fragmento de DNA artificial llamado cebador, mediante la acción de una enzima denominada DNA polimerasa.
El resultado es la duplicación del número de moléculas de una secuencia concreta de DNA.
Este proceso se repite un número determinado de veces o ciclos, generalmente 30, y se consigue un aumento o amplificación exponencial del número de copias del fragmento de DNA molde. Por tanto, si partimos de una molécula única de DNA en la muestra inicial, y en cada ciclo se duplica el número de moléculas, teóricamente, al final de los 30 ciclos, se obtendrán 230 moléculas idénticas, es decir 1073741824 moléculas.
Conceptualmente, la PCR es una técnica sencilla, consiste en la separación por calor de las dos cadenas del DNA que se quiere amplificar, y su copia simultánea a partir de un punto, determinado por un fragmento de DNA artificial llamado cebador, mediante la acción de una enzima denominada DNA polimerasa.
El resultado es la duplicación del número de moléculas de una secuencia concreta de DNA.
Este proceso se repite un número determinado de veces o ciclos, generalmente 30, y se consigue un aumento o amplificación exponencial del número de copias del fragmento de DNA molde. Por tanto, si partimos de una molécula única de DNA en la muestra inicial, y en cada ciclo se duplica el número de moléculas, teóricamente, al final de los 30 ciclos, se obtendrán 230 moléculas idénticas, es decir 1073741824 moléculas.
La
gran ventaja de la PCR es que amplifica únicamente el fragmento de DNA que
queremos aunque esté en cantidades mínimas (alta sensibilidad) o en presencia de grandes cantidades de otros
DNA semejantes (alta especificidad).
La reacción es eficaz incluso si se parte de muestras de DNA muy poco purificadas, en presencia de otros componentes.
La reacción es eficaz incluso si se parte de muestras de DNA muy poco purificadas, en presencia de otros componentes.
La PCR
mejoró vertiginosamente como herramienta de laboratorio a partir de 1988,
gracias a dos hechos que hicieron que la técnica se pudiera automatizar: el
primero de ellos fue la comercialización de la enzima denominada Taq
polimerasa (Saiki et al, 1988) que es un enzima termoestable, por lo que
permanece activa después de incubaciones prolongadas a 94 ºC, y no hay que
añadirla en cada ciclo de amplificación.
El segundo hecho fue la aparición en el mercado de los primeros termocicladores que realizaban los cambios de temperatura automáticamente, sin necesidad de distintos baños. La gran revolución que ha producido en la Biología Molecular la aparición de la PCR ha supuesto para su descubridor la concesión del Premio Nobel en el año 1993.
El segundo hecho fue la aparición en el mercado de los primeros termocicladores que realizaban los cambios de temperatura automáticamente, sin necesidad de distintos baños. La gran revolución que ha producido en la Biología Molecular la aparición de la PCR ha supuesto para su descubridor la concesión del Premio Nobel en el año 1993.
Así, la
PCR se ha convertido en una herramienta fundamental en campos tan diversos
como la investigación (clonado de genes, detección de clones recombinantes,
estudio de DNA de fósiles), medicina forense y criminalística (determinación
de la paternidad, identificación de individuos, identificación
sospechoso/evidencia en casos de asesinato, violación, etc.), sanidad animal y
mejora genética (detección de enfermedades genéticas e infecciosas, pureza de
razas, etc.) y medicina (diagnóstico de enfermedades).
La PCR fue desarrollada por Kary Mullis (Saiki et al, 1985; Mullis, 1990) en 1985, utilizando como DNA polimerasa el fragmento Klenow de la DNA polimerasa I de E. coli y lo llevó a cabo cambiando los tubos de reacción en cada ciclo, entre dos baños que estaban a 94 ºC (desnaturalización) y 37 ºC (hibridación y extensión del cebador). Debido a que esta enzima se desnaturaliza a temperaturas superiores a 37 ºC, era necesario añadirla en cada uno de los ciclos tras el paso de desnaturalización, lo que convertía a la PCR en una técnica tediosa y costosa. |
4.4.1 SECUENCIACION DEL ADN
Secuenciacion de los
Acidos Nucleicos
La introducción de métodos rápidos de secuenciación a finales de los años 70 representó un cambio importante en los estudios sobre el DNA Existen TRES métodos de secuenciación de los ácidos nucleicos.
Uno de ellos (Maxam y Gilbert) utiliza reactivos químicos a fin de cortar el DNA a nivel de bases específicas. El otro se denomina enzimático, de terminación en cadena o didesoxi (Sanger, Nicklen y Coulson). Y actualmente el metodod automatizado con lectores laser de capilaridad. El fin de ambos es conseguir la secuencia completa de cada una de las bases que constituyen un fragmento de ácido nucleico.
En el método químico un fragmento de DNA se marca en uno de sus extremos con P o S
radiactivo por acción de la enzima polinucleótido quinasa. Ambos extremos se
separan por la acción de una enzima de restriccion.
El paso siguiente consiste en romper estos fragmentos, no más de una o dos veces por molécula, con reacciones químicas específicas para cada una de las cuatro bases. Haremos cuatro alícuotas y trataremos cada una de ellas con un compuesto químico que modifique una de las cuatro bases, aproximadamente una vez por molécula de DNA. El tratamiento posterior con piperidina producirá la rotura de la cadena allí donde la base había sido alterada.
El paso siguiente consiste en romper estos fragmentos, no más de una o dos veces por molécula, con reacciones químicas específicas para cada una de las cuatro bases. Haremos cuatro alícuotas y trataremos cada una de ellas con un compuesto químico que modifique una de las cuatro bases, aproximadamente una vez por molécula de DNA. El tratamiento posterior con piperidina producirá la rotura de la cadena allí donde la base había sido alterada.
Especificidad
Base Reactivo
G Dimetil
sulfoxido
G+A Acido
fórmico
T Permanganato
Potásico
C Hidroxilamina
Posteriormente se analizan los fragmentos en geles desnaturalizantes.
Actualmente para el marcaje se
utilizan cuatro fluorocromos distintos: fluoresceina,
NBD(4-cloro-7nitrobenceno-2oxal-diazol), tetrametilrodamina y rojo texas, uno
para cada base.
Una vez conjugados a cuatro alícuotas del cebador, se procede a la extensión del iniciador e interrupción con dideoxis.
Una vez conjugados a cuatro alícuotas del cebador, se procede a la extensión del iniciador e interrupción con dideoxis.
Geles
de secuenciación
Método
enzimático de terminación de cadena o método didesoxi de Sanger
Para obtener la secuencia de bases nitrogenadas de un
segmento de ADN por el método enzimático de terminación de cadena, se necesitan
los siguientes compuestos:
El ADN molde o segmento de
ADN que se desea secuenciar. Para poder secuenciar un segmento de ADN,
previamente se necesita tener gran cantidad de ese fragmento, y por tanto, hay
que clonarlo en un vector apropiado. Además, debe estar en estado de hélice
sencilla.
Un enzima que replique el ADN, normalmente
la ADN Polimerasa I del bacteriofago T4. La ADN Polimersa I del fago T4 emplea
como molde ADN de hélice sencilla y siguiendo las reglas de complementaridad de
las bases nitrogenadas va añadiendo nucleótidos a partir de un cebador o
"primer".
Un cebador o "primer" que suele
ser un oligonucleótido corto de alrededor de 20 bases de longitud necesario
para que la ADN polimerasa I comience a añadir nucleótidos por el extremo 3'
OH.
Este cebador debe poseer una secuencia de bases complementaria a la del fragmento de ADN que se desea secuenciar.
Debido a que la secuencia de nucleótidos del segmento que se quiere secuenciar es desconocida, se emplea un "primer" con secuencia complementaria al vector empleado para clonar el fragmento de ADN, además, este cebador procede de una región del vector muy cercana al punto de inserción del ADN problema cuya secuencia se conoce.
El "primer" utilizado suele marcarse radiactivamente.
Este cebador debe poseer una secuencia de bases complementaria a la del fragmento de ADN que se desea secuenciar.
Debido a que la secuencia de nucleótidos del segmento que se quiere secuenciar es desconocida, se emplea un "primer" con secuencia complementaria al vector empleado para clonar el fragmento de ADN, además, este cebador procede de una región del vector muy cercana al punto de inserción del ADN problema cuya secuencia se conoce.
El "primer" utilizado suele marcarse radiactivamente.
Los cuatro nucleótidos trifosfato
(dATP, dCTP, dGTP y dTTP). A veces en vez de marcar radiactivamente el cebador,
se marca radiactivamente uno de los cuatro nucleótido trifosfato en cada
reacción.
Por último, se necesitan nucleótidos
didesoxi (ddATP, ddTTP, ddCTP y ddGTP). Los nucleótidos didesoxi son
nucleótidos modificados que han perdido el grupo hidroxilo de la posición 3'
de ladesoxirribosa.
Por último, se necesitan nucleótidos didesoxi (ddATP,
ddTTP, ddCTP y ddGTP). Los nucleótidos didesoxi son nucleótidos modificados que
han perdido el grupo hidroxilo de la posición 3' de la desoxirribosa.
Estos nucleótidos pueden incorporarse a la cadena de ADN naciente, pero no es posible que se una a ellos ningún otro nucleótido por el extremo 3'. Por tanto, una vez incorporado un nucleótido didesoxi se termina la síntesis de la cadena de ADN.
Breve
descripción del método enzimático de terminación de cadena
por ejemplo ddATP, a una concentración baja. El nucleótido didesoxi utilizado (ddATP en este ejemplo) competirá con su homólogo (dATP) por incorporarse a la cadena de ADN que se está sintetizando, produciendo la terminación de la síntesis en el momento y lugar donde se incorpora. |
Los fragmentos de ADN de nueva síntesis obtenidos en cada mezcla de
reacción se separan por tamaños mediante electroforesis en geles verticales de
acrilamida que permiten distinguir fragmentos de ADN que se diferencian en un
solo nucleótido.Los productos de cada una de las cuatro mezclas de reacción se
insertan en cuatro carriles diferentes del gel.
Una vez terminada la electroforesis, el gel se pone en contacto con una
película fotográfica de autorradiografía.
La aparición de una banda en una posición concreta de la autorradiografía en una de las cuatro calles nos indica que en ese punto de la secuencia del ADN de nueva síntesis (complementario al ADN molde) está la base correspondiente al nucleótido didesoxi utilizado en la mezcla de reacción correspondiente.
La aparición de una banda en una posición concreta de la autorradiografía en una de las cuatro calles nos indica que en ese punto de la secuencia del ADN de nueva síntesis (complementario al ADN molde) está la base correspondiente al nucleótido didesoxi utilizado en la mezcla de reacción correspondiente.
Teniendo en cuenta
que el ADN de nueva síntesis crece en la dirección 5' ® 3', si comenzamos a
leer el gel por los fragmentos de menor tamaño (extremo 5') y avanzamos
aumentando el tamaño de los fragmentos (hacia 3'), obtendremos la secuencia del
ADN de nueva síntesis en la dirección 5' -- 3'.
Breve
descripción del método automático de secuenciación
La principal
diferencia entre método enzimático de terminación de cadena y el método
automático de secuenciación radica, en primer lugar en el tipo de marcaje.
En el método automático en vez de radiactividad se utiliza fluorescencia y lo habitual es realizar cuatro mezclas de reacción, cada una con nucleótido trifosfato (dTTP) marcado con un fluorocromo distinto.
Este sistema permite automatizar el proceso de manera que es posible leer al mismo tiempo los ADNs de nueva síntesis producto de las cuatro mezclas de reacción.
En el método automático en vez de radiactividad se utiliza fluorescencia y lo habitual es realizar cuatro mezclas de reacción, cada una con nucleótido trifosfato (dTTP) marcado con un fluorocromo distinto.
Este sistema permite automatizar el proceso de manera que es posible leer al mismo tiempo los ADNs de nueva síntesis producto de las cuatro mezclas de reacción.
La segunda diferencia
radica en el sistema de detección de los fragmentos de ADN.
La detección del tipo de fluorescencia correspondiente a cada reacción se lleva a cabo al mismo tiempo que la electroforesis, de manera que los fragmentos de ADN de menor tamaño que ya han sido detectados se dejan escapar del gel, permitiendo este sistema aumentar el número de nucleótidos que se pueden determinar en cada electroforesis y, por consiguiente, en cada secuenciación.
La detección del tipo de fluorescencia correspondiente a cada reacción se lleva a cabo al mismo tiempo que la electroforesis, de manera que los fragmentos de ADN de menor tamaño que ya han sido detectados se dejan escapar del gel, permitiendo este sistema aumentar el número de nucleótidos que se pueden determinar en cada electroforesis y, por consiguiente, en cada secuenciación.
El siguiente
esquema representa de forma abreviada el método automático de secuenciación
BIBLIOGRAFIA:
- Bramhill, D., and Kornberg, A. 1988. A model for initiation at origins of DNA replication. Cell 54:915-18.